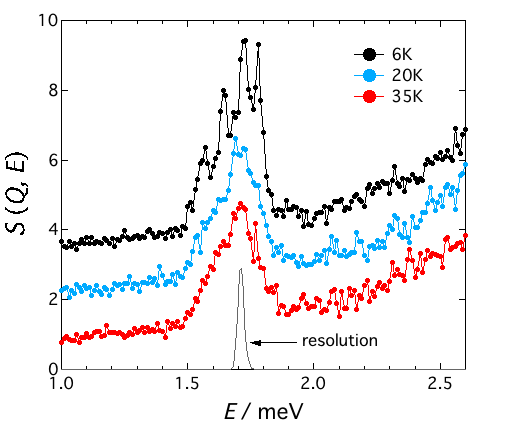
"ガラス"というと皆さんは窓や食器などに使われている透明で硬いものを思い浮かべると思いますが,これは SiO2 を主成分とするガラスです。化学物理の世界のガラスは,もっと広義の言葉で,液体が低温(あるいは高圧)で流動性をなくし無秩序な構造のまま固まった状態の総称です。図1に物質の構造とエントロピー(あるいは体積)の温度変化を模式的に示しました。この図から明らかなように,液体を過冷却させることができれば最後は必ずガラスに成ります。ガラスは特殊なものと思われがちですが,実はどのような物質にも現れる「物質の第4の状態」と言えるものなのです。液体がガラスになる過程を「ガラス転移」と呼びます。このメカニズムについては,古くから多くの科学者が研究してきましたが未だ分かっておらず,解明されればノーベル賞は確実と言われています。さらに,ガラスには構造緩和の非線形性,低エネルギー励起(ボゾンピーク)など構造不規則性に由来する様々な興味深い現象があります。我々の研究室では,低分子ガラスに焦点を絞って,これらの謎の解明に挑戦しています。
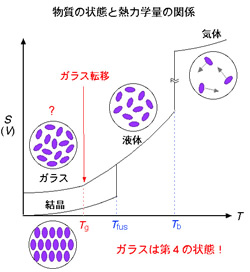
私たちは通常の冷却では結晶化してしまう単純な分子をガラスにする方法「低温蒸着法」を開発しました(「Instruments」の項参照)。この方法で得られる冷却速度は,107K/sに相当します。図2にプロットしたのはこの方法で得られたプロペン分子ガラスの熱容量です。注目して欲しいのは55K付近に現れるガラス転移です。55Kという温度はこれまでに観測されたガラス転移の中で最低ですし,熱容量ジャンプの大きさはこれまでで最大です(ガラスと液体の熱容量比にして2.5倍)。ガラスと液体の熱容量差を積分すると構造エントロピーという量が得られますが,これを詳しく解析することで,ガラス転移付近では10分子程度が協同的に運動していることが明らかになりました。このかたまりはCRR(Cooperatively Rearranging Region)と呼ばれ,ガラス転移の謎を解く鍵になると考えられています。
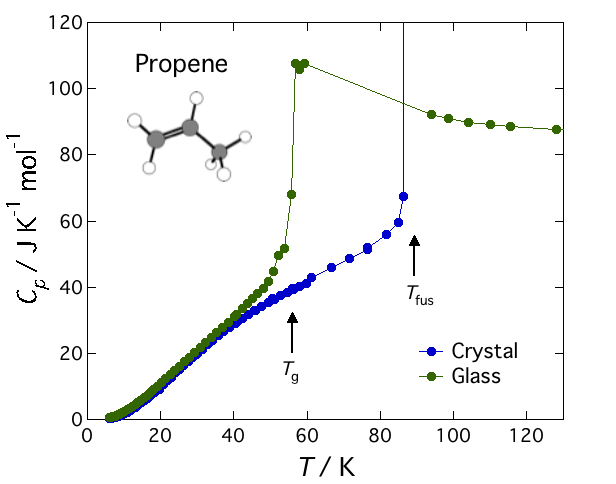
CRRの問題に限らず,ガラスの構造を詳しく知ることは,ガラスの研究で最も基本的なことです。図3は低温蒸着法で作成した四塩化炭素ガラスの中性子回折データです。四塩化炭素分子(CCl4)はこれまでに構造解析がなされた分子ガラスの中では最も単純な分子構造(正四面体)をしています。分子配向相関の解析から,四塩化炭素ガラスの中では3つの分子が図中にあるように規則正しく並んでいることが分かりました。もちろん,このような秩序構造は局所的なもので,ガラス全体をみれば,やはりガラスの構造は無秩序になっています。最近,同じ方法を用いて直線分子であるCS2のガラス化にも成功しました。これからどんどん装置の改良を進め,最終的には窒素(N2)やアルゴン(Ar)のような極めて単純な分子のガラスを作り出すことが私たちの夢です。
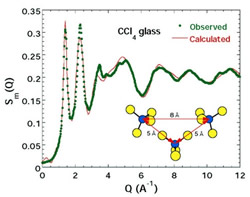
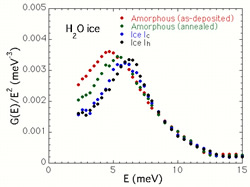
図4は私たちが中性子非弾性散乱という方法で測定した水のガラス(アモルファス氷とも呼ぶ)の振動状態密度です。結晶やガラスは様々な固有振動数をもつバネの集合体として近似できるのですが,振動状態密度とはその振動数の分布を表すものです。アモルファス氷は結晶氷に比べてはるかに低い振動数の励起(低エネルギー励起)を起こすこと,またガラス転移温度付近でアニールするとその励起強度が減少することがこのデータから明らかになりました。現在,この異常の起源を探るため,希ガスやアルコールなど色々な分子を溶かし込んだアモルファス氷の測定を行っています。
図1:物質の構造とエントロピー(あるいは体積)温度変化
図2:プロペンの熱容量
図3:四塩化炭素ガラスの中性子回折パターンと理論曲線
図4:水のガラスの振動状態密度
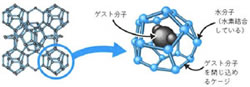
最近,テレビや新聞でメタンハイドレートという物質が話題になっています。この物質はクラスレート化合物(包接化合物)と呼ばれる物質の仲間で,図5で示したような水分子のケージ状構造にメタン分子(CH4)が取り込まれた結晶です。話題になっているのは,メタンハイドレートが日本近海の海底に多量に存在することが分かり,その中からメタンを効率よく取り出す方法が見つかれば,約100年分の天然ガス資源になると推定されているからです。外見は氷とそっくりですが,温度が上がるとメタンガスが発生しますので,マッチで火をつけると図6のようによく燃えます。「燃える氷」と呼ばれているのはそのためです。メタン以外にも色々な分子(ゲスト分子と呼びます)がクラスレートハイドレートになることが知られており,二酸化炭素を海底に固定したり,国外で採取した天然ガスをハイドレートにして日本に輸送するなどの応用も考えられています。
我々が興味をもっているのは,もちろんそのような応用ではなく,クラスレートハイドレートの分子運動とクラスレートハイドレートの生成メカニズムです。ケージの中でゲスト分子はどのように廻っているのでしょうか?ゲスト分子と水分子の運動の相関は?そもそも,ゲスト分子を溶かし込むだけで上図のような複雑な構造の結晶が一体どのようにしてできるのでしょうか?それらの謎を解く第一歩として,最近我々は,メタンハイドレートの熱容量を測定しました。また,ハイドレートができる前の溶液状態の中性子準弾性散乱の研究を行いました。
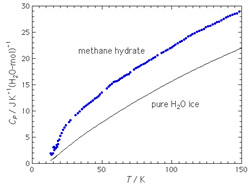
メタンハイドレートは低温・高圧下でしか安定に存在しないため,これまで誰も熱容量を測定することができませんでした。今回私たちは,つくばの産総研(山本佳孝研究室)で合成された試料を80Kで保持しながら私たちの実験室まで運び,内部をあらかじめ80Kに冷やしておいたトップローディング式カロリメーター(「Instruments」の項参照)にセットしました。図7は世界で初めて測定されたメタンハイドレートの熱容量です。氷の熱容量と比べると,ゲスト分子の分だけ熱容量が大きくなっています。この熱容量を詳しく解析することにより,ゲスト分子はケージの中でほとんど自由に回転していることが分かりました。
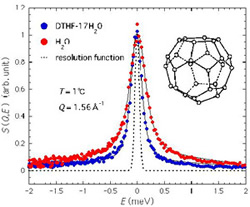
図8に,中性子準弾性散乱スペクトルの一例として,1℃におけるH2OとD化テトラヒドロフラン(THF)水溶液のデータをお見せします。THF分子は水に良く溶け簡単にハイドレートを作ります。全く水分子が拡散運動をしていないときはスペクトルは図8中の破線のようなシャープなピークになりますが,拡散運動が盛んになるとピークがどんどんブロードになります。このデータをローレンツ関数でフィットし,その線幅を跳躍拡散モデルで解析することにより水分子の拡散係数を計算しました。同様のことを他の温度,他のゲスト分子に対しても行いました。ゲスト分子の水溶液中の水分子拡散の活性化エネルギーは,純水中よりはるかに大きくなることが分かりました。このことは,溶液状態でもゲスト分子を取り囲むようにケージ様な局所構造が存在しており,水分子の拡散が阻害されているためであると考えています。
THFなどの有機ゲスト分子は構造が複雑であるため,どうしても水分子運動の議論が曖昧になりがちでした。そこで,最近導入した気体高圧発生装置(「Instruments」の項参照)を用いて,ゲスト気体を水に強制的に溶解させ,上と同様の中性子準弾性散乱実験を行いました。メタンなどの無極性分子は大気圧下では水にほとんど溶けませんが,圧力を100 MPa(約1000気圧)にすると2%程度水に溶け込みます。
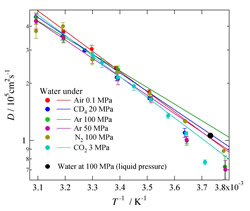
図9はその結果得られた拡散係数のアレニウスプロットです。高温では通常の水の拡散係数とほとんど変わりませんが,低温にするほど拡散係数はどんどん小さくなります。このことは100 MPaのバルク水のデータ(図中の黒丸)を比べるとよく分かります。また,拡散係数の減少は,水に溶けやすい気体分子(二酸化炭素)ほど顕著です。この結果は,先に示したTHF水溶液などの場合と同じくゲスト分子周りにケージ様な局所構造が存在することを示しています。今後,この研究を進め,気体水和物の生成機構を追求していく予定です。
図5:クラストレート化合物のケージ状構造
図6:メタンハイドレート
図7:メタンハイドレートの熱容量
図8:テトラヒドロフラン(THF)水溶液の準弾性散乱スペクトル
図9:気体高圧下での水分子の拡散係数のアレニウスプロット
最近,イオン液体(あるいは常温イオン液体)と呼ばれる一連の物質が注目を集めています。通常,イオン性化合物は室温では固体なのに(例えばNaClの融点は800℃),イオン液体は室温で安定な液体として存在します。イオン液体は低蒸気圧,不燃性,高イオン伝導性などの性質があるため,新しい環境調和型溶媒や電池材料として応用面で注目されていますが,ガラス転移を中心とした基礎物性研究の立場からも重要な対象です。
すでに様々な種類のイオン液体が開発されていますが,図10は典型的な陽イオンである1-ブチル-3-メチルイミダゾリウムイオン(C4mimイオンと略します)の構造図です。これまでに私たちは,このようなイミダゾール環を有する陽イオンのイオン液体に対して,アルキル基の長さや陰イオンを変化させて,熱容量と中性子準弾性散乱を測定してきました。サンプルは東大院理の浜口研究室と横国大化学分析室の中越先生から提供してもらっています。
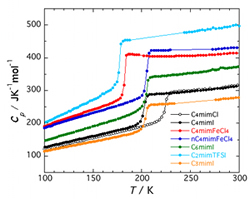
図11はイオン液体を急冷して得られるガラスの熱容量データです。どの試料においても,180-220Kで大きな熱容量のジャンプを伴うガラス転移が起こることが分かりました。ガラス転移温度以上の大きな過剰熱容量は,イオン液体が分子液体と同様にFragile液体(構造が乱れており,それが顕著に温度変化する)であることを示しています。イオン液体の主たる相互作用は強く長距離的であるクローン力です。そのため,イオン液体の局所構造はあまり温度変化しないと考えていたのですが,今回の結果は全く予想外でした。
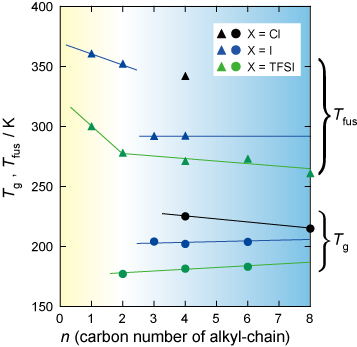
図12にアルキルイミダゾリウム系イオン液体のアルキル鎖の炭素数nに対してガラス転移温度と融解温度をプロットしました。n=2以下の陽イオンではガラス転移は起こさず,融点も高温側に大きくシフトしました。n=3以上では,不思議なことに,融点もガラス転移温度もほとんど変化しません。この結果から,nが2と3の間に通常のイオン性結晶からイオン液体へのクロスオーバーがあると考えられます。また,陰イオンを大きくするほどガラス転移温度が低くなることもわかりました。以上の結果から,イオン液体の低融点の起源には,イオンの嵩高さからクーロン相互作用が弱くなっていること以外に,アルキル鎖の乱れ(配置エントロピーの増大)が深く関わっていると考えています。
図10:1-ブチル-3-メチルイミダゾリウムイオンの構造
図11:イオン液体のガラス状態の熱容量
図12:陽イオンのアルキル鎖の炭素数nに対するガラス転移温度と融解温度
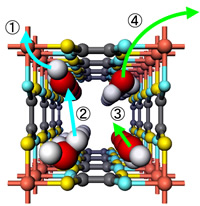
プロトン伝導体は,単に燃料電池の電解質としてだけでなく,様々なエネルギー貯蔵・変換機能デバイスにおいて重要な役割を果たします。安定性,軽量性,経済性などの様々な要求を満たすべく,世界中で日夜プロトン伝導体の研究が行われています。我々も京大院理の北川グループと共同で,新しいタイプのプロトン伝導体の研究を行っています。図13に局所構造を示したルベアン酸銅水和物(CuC2N2S2H2-nH2O)は,高いプロトン伝導性をもつ多孔性配位高分子錯体です。この物質の特長は,相対湿度を変化させることで細孔中に水を可逆的に吸収・放出し,プロトン伝導度を4桁も変化させることです。最大水分量(CuC2N2S2H2-3.4H2O)におけるプロトン伝導度は0.01 S/cmと非常に大きく,実用されている代表的なプロトン伝導体であるナフィオン膜と同程度です。我々の研究の目的はプロトン伝導の機構,特に水分子の役割を調べることです。
これまでに3種類のルベアン酸銅水和物および水素をヒドロキシエチル基で置換したルベアン酸銅水和物の中性子散乱測定を行いました。弾性非干渉性構造因子(EISF)の解析から,水分子は結晶の中を動き回るのではなく,psオーダーの時間スケールでは細孔内の空間にトラップされていることが分かりました(上の構造図中の(4)の過程は行っていない)。また,跳躍拡散モデルの解析から,水分子の自己拡散係数を得ました。図14はルベアン酸銅の細孔内に存在する水分子の自己拡散係数の温度変化です。水分量が増加するほど自己拡散係数が増加し,水分子がプロトンのキャリアーであることが明確になりました。非常に興味深いのは,活性化エネルギーの値が8 kJ/molとバルク水(17 kJ/mol)と比べてかなり小さくなっていることです。また,跳躍距離について解析を行ったところ,バルク水(0.8Å)と比べてはるかに長い1.3Å程度であることが分かりました。これらの結果は,細孔の壁の影響で水分子が隣の水分子と理想的な距離・角度の水素結合を形成できないことに起因すると考えられます。以上の結果から,ルベアン酸銅水和物におけるプロトン伝導機構は,いわゆるGrotthuss機構であり,(1)の過程で供給されたプロトンが,細孔内水分子の局所的拡散((3)の過程)と水分子間のプロトン移動((2)の過程)により運ばれることが明らかになりました。
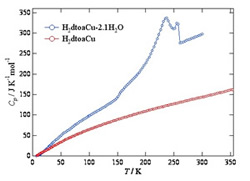
次に,ルベアン酸銅の乾燥試料および中間の水分子量の含水試料(CuC2N2S2H2-2.1H2O)の熱容量を測定しました(図15参照)。乾燥試料では熱異常は見られませんが,含水試料では150 K付近に熱容量の段差を伴うガラス転移が,150-260 Kの広い温度範囲にブロードなピークが観測されました。ガラス転移は,この温度以上では水分子が熱容量の観測時間スケール(100 s程度)で動いていることを意味しています。水分子が150Kという低温まで動き続けていることは通常はあり得ないことで,非常に興味深い現象です。また,エントロピーの解析から,ブロードなピークが,固体状態になった水分子が温度を上げるとともに徐々に融解していく過程によることが分かりました。
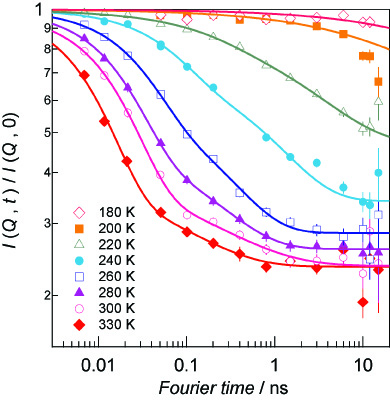
図16はNIST(USA)の中性子スピンエコー装置で測定したルベアン酸銅水和物の中間散乱関数の温度変化です。図14で観ている領域も含む広い時間領域の水分子の運動を観測しています。転移温度より高温の260K以上では2種類の緩和が,240K以下では単一の緩和が観測されています。緩和量に関する解析から,260Kの相転移は,図14で観ている自由な(動きやすい)水分子が細孔壁に凝縮する非常に興味深い相転移であることが分かりました。
図13:ルベアン酸銅水和物の局所構造
図14:ルベアン酸銅水和物中の水分子の拡散係数のアレニウスプロット
図15:ルベアン酸銅水和物の熱容量
図16:ルベアン酸銅水和物の中間散乱関数
我々が通常”磁石”と呼んでいるものは,原子の磁気モーメントが揃っている物質(強磁性体)のことを指します。強磁性体と言っても,物質中の全ての磁気モーメントが揃っているわけではなく,物質内でいくつかの領域(磁区)に分かれており,それぞれの磁区内で磁気モーメントが揃っています。そこに強い磁場を印加すると磁区を隔てている磁壁が移動し,物質全体の磁気モーメントが一方向に揃います。"磁石"ができるのです。いったん揃うと磁場をゼロにしても元には戻りません。これは磁壁が動くにはエネルギー障壁があるからです。これを"保磁力"と言います。
単分子磁石(Single-Molecule Magnet)では,1つの分子があたかも磁区であるように振る舞い,保磁力を持ちます。強磁性体磁石と比べるとはるかに小さな磁区(分子)ですし,1つ1つの分子は孤立しており磁壁もありません。
単分子磁石の磁気モーメントと保磁力の起源は何なのでしょうか?
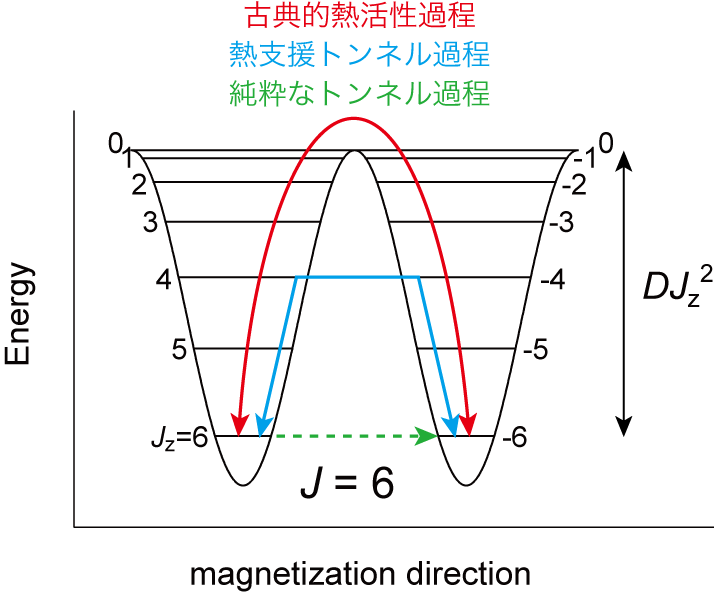
単分子磁石では,幾つかの磁性イオンがクラスターを形成し,クラスター内の磁気モーメントの和がクラスター(分子)の磁気モーメントとなります。この場合,大雑把に書くとそのエネルギーはDJz2で表されます。Jzは磁気モーメントのz成分であり,Dは一軸異方性パラメーターと呼ばれます。D<0の場合は磁気モーメントがz方向に向いた状態が安定になります。ここで,x, y成分は無視しています(これをイジングスピンといいます)。図17はJ=6の場合の磁気モーメントの方向に対するエネルギーです。Jz=6(上向きモーメント)からJz=-6(下向きモーメント)に反転するためにはDJz2の高いポテンシャル障壁を超えなければなりません。これが保磁力の起源です。一般に,磁化反転は遅い熱活性過程(古典的熱活性過程)によって起こります。
ただ,実際には,古典的な熱活性過程だけではなく,状態間のトンネリングによって磁化反転が起こることもあります(熱支援トンネル過程や純粋なトンネル過程)。このトンネル過程のメカニズムを探ることが現在の単分子磁石研究において最重要の課題です。
これまでは,MnやFeなどの3d遷移金属を含む単分子磁石が盛んに研究されてきました。これらの物質では,ひとつのクラスターに4〜12個くらいの磁性イオンが含まれています。
しかし最近,希土類元素を含む単分子磁石が開発され,注目を集めています。3d遷移金属に比べると希土類元素の磁気モーメントや磁気異方性は大きく,少ない磁性イオンで単分子磁石を形成するので,より正確な測定および解釈を可能にします。また,エネルギースケールが3d遷移金属のものより大きいため,ナノ磁気デバイスへの応用も期待されます。
現在我々が研究しているのは,TbイオンとCuイオンから成る二核錯体系です。この研究は,奈良女大の梶原グループと共同で行っています。
この物質系で面白いのは,Tbイオン周りの配位子のわずかな変化によって,単分子磁石から非単分子磁石へと変化することです。
我々はそれらのエネルギー準位を決定するために,中性子非弾性散乱実験を行いました。実験は,最近新設されたJ-PARC(茨城県東海村)のAMATERAS分光器を用いて行いました。
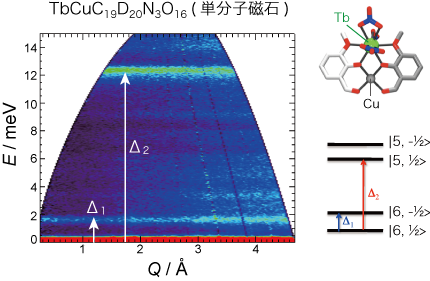
図18と図19に,単分子磁石と"非"単分子磁石の散乱強度マップを示します。横軸が散乱ベクトル,縦軸が遷移エネルギーです。単分子磁石と"非"単分子磁石では,明らかに散乱の様子が違っています。これらのデータを散乱強度のQ依存性も含めて解析することにより,エネルギースキームを決めました(マップの右に記載)。単分子磁石では,基底状態は|Jz=6, Sz=1/2>(JzはTbの磁気モーメント,SzはCuスピン)で,第一励起状態はCuスピンを反転した|Jz=6, Sz=-1/2>,第二励起状態はTbの磁気モーメントが変化した|Jz=6, Sz=1/2>であることがわかりました。基底状態から第一励起状態への遷移は,TbとCuの間の交換相互作用に起因するものであり,このエネルギーが交流磁化率から得られた活性化エネルギー(16K)とほぼ一致しています。また,さらに精密な測定を行ったところ,この励起は幾つかのピークに分裂していることがわかりました(図20)。これはTbの電子の磁気モーメントと核磁気モーメントとの間の相互作用によるもので,この相互作用により,トンネリングが起こっているのではないかと考えています。
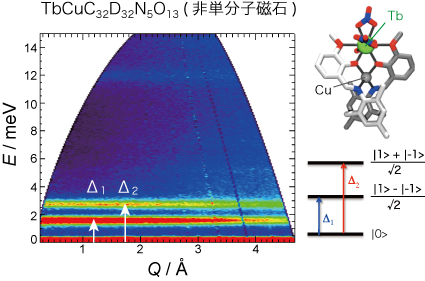
一方,非単分子磁石では,基底状態が|Jz=0>,第一,第二励起状態が(|Jz=1>±|Jz=-1>)/√2となっています。つまり,磁気モーメントはz方向ではなくxy面内に寝るのがエネルギー的に安定(容易面型)であり,これが単分子磁石にならない理由であることがわかりました。
今後は,エネルギー準位だけでなく,緩和挙動を直接中性子散乱で観測したいと考えています。また,単核の単分子磁石の測定も計画しています。
図17:エネルギーの磁化方向依存性
図18:Tb-Cu錯体(単分子磁石)の非弾性磁気散乱マップ
図19:Tb-Cu錯体(非単分子磁石)の非弾性磁気散乱マップ
図20:Tb-Cu錯体(単分子磁石)の磁気励起のエネルギー依存性

![[bmim]+ イオン](images/bmim_cation.jpg)